Введение. Большинство вариантов химиотерапии при раке молочной железы подразумевают внутривенное введение противоопухолевых препаратов. Однако, введение препаратов через вены, особенно на руках, не всегда проходит бесследно. Можно ли пройти через курс химиотерапии и сохранить здоровье вен?
Куда могут вводиться противоопухолевые препараты?
Большинство режимов химиотерапии при лечении рака молочной железы подразумевают введение противоопухолевых препаратов внутривенно, через предварительно установленный венозный доступ (катетер или порт-система). Для этих целей могут использоваться:
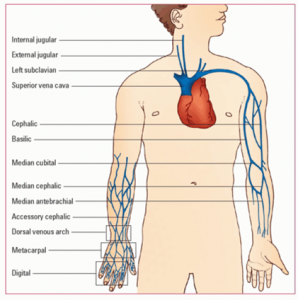
- центральные вены – это вены подключичной области, а также вены шеи (яремные вены)
- периферические вены – это вены рук: предплечья и локтевой ямки
Что насчет бедренной вены?
К центральным венам также относят вены на бедре. Однако, катетеризация и проведение терапии через бедренные вены небезопасны в силу высокого риска инфекционных и тромботических осложнений*. Катетеризация бедренной вены оправдана только в экстренных ситуациях для оказания неотложной помощи и при невозможности обеспечения венозного доступа через другие вены; в случае же плановой химиотерапии, бедренная вена – крайне неподходящий вариант для проведения данной процедуры.
* тромбоз – это состояние, при котором внутри сосуда формируется кровяной сгусток-тромб, вызывающий закупорку кровеносных сосудов. Тромб затрудняет либо делает невозможным дальнейший ток крови к органу, к которому проложен сосуд, что вызывает нарушение функции органа, иногда с весьма тяжелыми осложнениями.
Каким образом осуществляется внутривенное введение противоопухолевых препаратов
Для введения противоопухолевых препаратов через вены используются разные приспособления1,2.
- Одноразовые катетеры: для периферических вен на руках используются “периферические” катетеры, для подключичной и яремной вены – “центральные”.
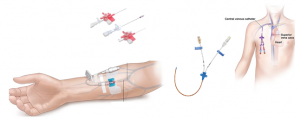
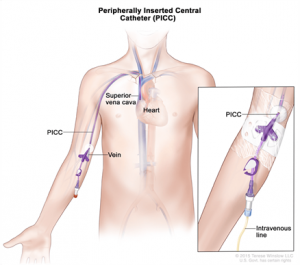
- ПИК-катетер (Периферически Имплантируемый центральный Катетер) – это приспособление, которое очень похоже по своей сути на центральный катетер, но, в отличие от последнего, имплантируемый в вену руки и пригодный для многократного использования, сроком до 6 месяцев. Конечная часть этого катетера достигает центральной вены, что делает введение химиопрепаратов безопасным.
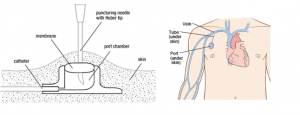
- Венозная порт-система – устройство, которое имплантируется под кожу и служит для многократных и длительных внутривенных введений. Оно состоит из специальной маленькой камеры с пластмассовым катетером (трубкой), который во время несложной операции соединяют с центральной веной. В самой камере есть мембрана, через нее можно ввести в камеру специальную иглу – иглу Губера – и осуществлять как введения препаратов, так и забор крови для анализов.
Какие риски при введении препаратов через периферические вены?
Флебиты. При введении химиопрепаратов через периферические вены возможно3,4,5 их воспалительное повреждение в виде флебита и тромбофлебита. Флебит вызывает такие симптомы, как боль, отек, покраснение и, в худшем случае, затвердение и склероз (“заращение”) вены, что приводит к пальпируемому венозному канатику. Иногда, вслед за флебитом возникает тромбоз6 вен верхних конечностей – тромбофлебит.
В наиболее тяжелых случаях симптомы флебита могут сохраняться в течение нескольких месяцев после завершения химиотерапии.
Экстравазация. При введении препаратов через вены на руках с помощью одноразовых катетеров существует риск экстравазации7,8,9 – выхода препаратов из вены в окружающие ткани. Риск особенно высокий в случаях:
- если ранее инъекции и введения препаратов в вены руки уже осуществлялись
- если вены рук исходно тонкие и хрупкие
- лимфостаза руки, например, после удаления лимфатических узлов подмышечной области
- ожирения
- если применяются препараты – “везиканты”, сами по себе способные “выходить” за пределы сосудов в мягкие ткани руки
- необходимости многочасового введения препаратов
- неудачного расположения катетера, его слабой фиксации
Сама экстравазация препаратов опасна повреждением мягких тканей руки: кожи, подкожной клетчатки, мышц.
Наиболее серьезные повреждения развиваются при экстравазации доксорубицина, эпирубицина, винорелбина – вплоть до омертвения мягких тканей – состояние, требующее хирургического лечения.
Таксаны (паклитаксел, доцетаксел), вызывают менее серьезные повреждения – как правило, это глубокие воспаления, иногда приводящие к отслоению верхних слоев кожи и ее изъязвлению. Описаны случаи некроза (омертвения)10 мягких тканей руки при экстравазации паклитаксела.
Карбоплатин при экстравазации вызывает жжение, покраснение кожи, поверхностные воспалительные изменения.
Такие препараты, как циклофосфамид, гемцитабин, при экстравазации обычно не вызывают значимого повреждения мягких тканей.
Тромбозы. Определенный риск существует и при использовании ПИК-катетеров: при их применении чаще возникает тромбоз вен, чем при использовании центрального венозного катетера, что тоже делает использование ПИК-катетера не самым оптимальным вариантом для проведения химиотерапии.
Какой способ внутривенного введения наиболее оптимален для проведения химиотерапевтического лечения?
Химиотерапия при раке молочной железы проводится месяцами, если речь об операбельном раке, и годами, когда речь идет о метастатическом раке.
С учетом сроков проведения лечения, а также риска, связанного с особенностями вводимых препаратов, большинству пациенток при лечении рака молочной железы требуется использования11,12 центральных вен. Наиболее удобным и оптимальным приспособлением выступает венозная порт-система, имплантируемая под кожу.
Оптимальным порт-систему делает то, что ее можно устанавливать на весь период лекарственного противоопухолевого лечения, а также то, что в большинстве случаев порт-система никак не влияет на быт человека. Вы можете заниматься привычными для себя видами активности, заниматься спортом, ходить на работу. К тому же сама порт-система обычно незаметна для окружающих.
Правда ли, что порт показан только при невозможности использования периферических вен?
Показаниями для установки порт-системы служит необходимость длительного (3 и более месяцев) химиотерапевтического лечения.
Доступна ли порт-система по ОМС?
В настоящее время в РФ предусмотрена возможность имплантации венозной порт-системы по ОМС в стационарных условиях. Оплата имплантации порт-системы страховыми компаниями медицинскому учреждению осуществляется в рамках определенной КСГ (клинико-статистической группы), что дает возможность ряду медицинских учреждений оказывать помощь в виде данной процедуры.
Однако выбранное вами учреждение должно принимать участие в территориальной программе государственных гарантий бесплатного оказания медицинской помощи и оказывать помощь в рамках ОМС. Узнать, какие организации оказывают помощь по ОМС в рамках территориальной программы госгарантий, можно на сайте региональных органов здравоохранения.
Резюме
Химиотерапевтические препараты чаще всего вводятся внутривенным путем. Для введения препаратов возможно использование вен на руках (периферические вены) и центральных вен – на шее либо под ключицей. Большинство препаратов, применяемых при раке молочной железы, могут вызвать серьезные повреждения вен рук – как повреждения самой вены, так и мягких тканей, окружающих вену.
Сроки химиотерапии и особенности химиопрепаратов делают центральные вены наиболее безопасным местом для их введения. Оптимальным приспособлением для длительного химиотерапевтического лечения является венозная порт-система, имплантируемая под кожу.
Порт-система может функционировать длительное время, не накладывая практически никаких ограничений на ваш образ жизни. Показанием для ее установки служит необходимость проведения множества циклов химиотерапии в течение нескольких месяцев. В настоящее время существует возможность установки порт-системы по ОМС в учреждениях, участвующих в территориальной программе государственных гарантий бесплатного оказания медицинской помощи.
