Введение
Несмотря на активное внедрение лекарственной терапии в стандарты лечения рака молочной железы (РМЖ), большинство случаев данного заболевания не обходится без хирургического лечения.
В данной статье мы поговорим о том, как принимается решение об объеме и характере хирургического вмешательства на разных стадиях РМЖ, как влияет объем операции на отдаленные результаты лечения и какие действия нужно предпринимать для снижения риска рецидива после операции.
Всегда ли больше – значит лучше?
Еще с XIX века, до появления эффективных вариантов лекарственного лечения и лучевой терапии, стандартным вариантом1,2 операции при раке молочной железы была операция по Холстеду. Этот вариант операции подразумевает удаление очень большого объема тканей:
– всей молочной железы;
– клетчатки подмышечной зоны, где располагаются подмышечные лимфоузлы;
– грудных мышц.
Результаты такой операции и качество жизни пациенток весьма сложно назвать удовлетворительными. Удаление столь большого объема тканей приводит к развитию осложнений:
– лимфатического отека руки – лимфедемы;
– неврологические нарушения в виде парестезии – стойких ощущения жжения и покалывания в зоне оперативного лечения;
– стойких и длительных2,3 болей в зоне выполненной операции;
– ограничения движения в руке на стороне операции.
Столь серьезные функциональные последствия операции Холстеда можно было бы оправдать низкой частотой рецидива и прогрессирования рака молочной железы. Однако, исследование4, проведенное Бернандом Фишером, продемонстрировало, что уменьшение объема операции при раке молочной железы до удаления только молочной железы, не оказывало неблагоприятного влияния на риск прогрессирования рака и на длительность жизни пациенток. Более того, была поставлена под сомнение целесообразность удаления лимфатических узлов – во всяком случае, у всех пациенток без разбора – так как их удаление тоже не влияло на длительность жизни пациенток, участвовавших в исследовании.
Несколько позднее было опубликовано несколько работ, которые показали:
– Возможность в некоторых случаях удаления лишь части молочной железы, пораженной опухолью, при условии последующего5 проведения послеоперационной лучевой терапии (органосохраняющая резекция).
– Возможность выполнения в отдельных случаях менее травматичных вмешательств на лимфатические узлы в виде биопсии сигнальных лимфоузлов, селективной лимфодиссекции (когда удаляется лишь часть лимфоузлов подмышечной зоны).
Важно подчеркнуть, что возможность выполнения операций уменьшенного объема стало возможным благодаря развитию других видов лечения – лекарственной и лучевой терапии, которые активно применяются при неметастатическом раке молочной железы.
Какие варианты хирургического лечения применяются сегодня
Все варианты хирургического лечения различаются по объему проводимого вмешательства.
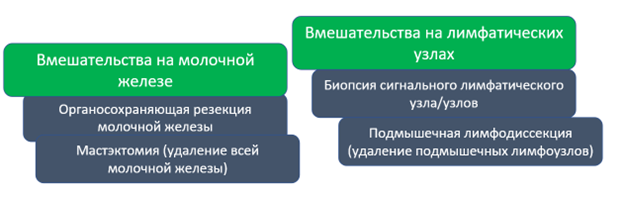
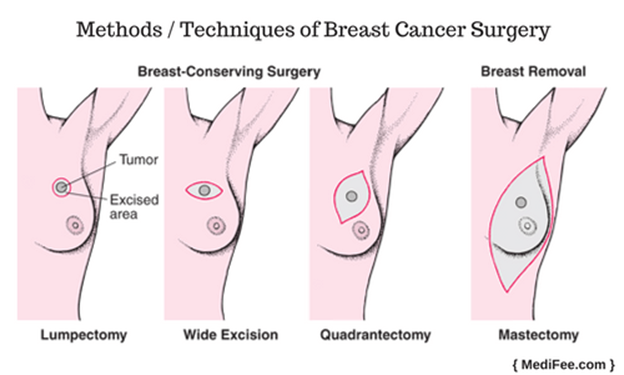
– Органосохраняющая резекция – удаление лишь части молочной железы, которая поражена опухолью.
– Мастэктомия – удаление всей молочной железы.
– Биопсия сигнального лимфоузла – процедура удаления лимфатического узла, накапливающего контрастное либо радиоактивное вещество, предварительно введенное пациентки перед операцией.
– Лимфаденэктомия или полная подмышечная лимфодиссекция заключается в удалении всех лимфатических узлов подмышечной зоны.
Как решается вопрос об объеме операции: органосохраняющая операция или мастэктомия
Органосохраняющая операция не реализуема и не предлагается в следующих6,7 ситуациях:
– заболевание имеет отечно-инфильтративную или маститоподобную форму;
– ранее была проведена лучевая терапия на зону пораженной молочной железы (например, по поводу лимфомы Ходжкина);
– ранее предпринималась попытка органосохраняющей операции, но она закончилась нерадикальным удалением опухоли;
– первый триместр беременности пациентки (при котором невозможно проведение послеоперационной лучевой терапии);
– невозможность проведения послеоперационной лучевой терапии.
Есть еще ряд ситуаций, при которых проведение органосохраняющей операции может быть затруднительным либо менее целесообразным:
– наличие двух и более опухолевых очагов в одной молочной железе;
– слишком большой размер опухоли молочной железы, при котором органосохраняющее удаление опухоли приведет к неудовлетворительным косметическим результатам;
– наличие наследственных мутаций, например BRCA1 и BRCA 2, при которой оправдано выполнение профилактической двусторонней мастэктомии.
Во всех остальных случаях вам может быть предложено органосохраняющее лечение. Возможность ее выполнения обосновываются тем, что результаты органосохраняющей операции и мастэктомии сопоставимы, если:
- Органосохраняющая операция дополняется послеоперационной лучевой терапией на зону вмешательства, что осуществляется у большинства пациенток, за некоторым исключением.
- Вы подходите под критерии, которые делают возможным проведение именно данного вмешательства.
Как решается вопрос об объеме операции: биопсия сигнальных лимфоузлов и лимфодиссекция
Отсутствие метастазов по УЗИ или КТ, выполненных перед операцией, не всегда гарантирует отсутствие опухолевых клеток в лимфоузлах, которые способны привести к рецидиву рака. Поэтому, при отрицательном результате УЗИ проводится уточняющее исследование – биопсия сигнального лимфоузла.
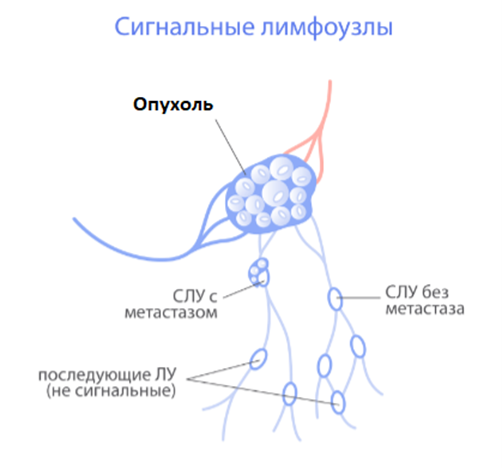
Сигнальный лимфоузел – тот лимфатический узел, который располагается к опухоли молочной железы наиболее близко. Чтобы найти его, в зону, близкой к расположению опухоли вводится8,9 специальный, безопасный для организма, радиофармпрепарат. В течение суток после его введения проводится операция по удалению опухоли молочной железы и по поиску и удалению сигнального лимфатического узла.
В условиях операционной врач с помощью специального датчика находит тот узел, в котором накопление препарата наиболее высокое – это и есть сигнальный лимфоузел. Такой узел подлежит хирургическому удалению и исследованию под микроскопом.
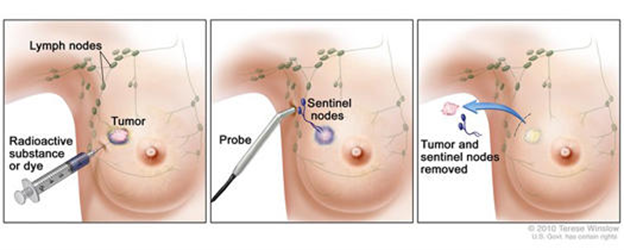
Дальнейшие шаги по вмешательству на лимфоузлы определяются9 результатами биопсии.
- Отсутствие метастазов либо обнаружение одного-двух метастазов не выступают показаниями для удаления всех лимфатических узлов, так как оно не приводит к снижению риска рецидива рака.
- Три и более метастаза в лимфоузлах по российским9 и зарубежным10 рекомендациям выступают поводом как для удаления лимфоузлов подмышечной зоны, так и для последующей послеоперационной лучевой терапии.
Когда приходится идти на удаление лимфатических узлов подмышечной области – подмышечную лимфодиссекцию
- Невозможность выполнения биопсии сигнальных лимфоузлов. К сожалению, далеко не во всех учреждениях нашей страны, есть условия для выполнения биопсии сигнальных лимфоузлов. В связи с этим, в российских клинических рекомендациях, предусмотрена необходимость выполнения лимфодиссекции при невозможности выполнения биопсии сигнальных лимфоузлов, если особенности опухоли пациентки (трижды негативный или HER2-позитивный подтип, поздняя стадия опухоли и ее высокая злокачественность по данным гистологического исследования) свидетельствуют о высоком риске рецидива заболевания.
- Наличие хотя бы одного метастаза в лимфоузлах после проведенной предоперационной химиотерапии. Научные данные, которые свидетельствовали бы о безопасном отказе от лимфодиссекции в этой ситуации, отсутствуют11.
- В случае, если пациентке, при наличии метастазов в лимфоузлах не проведена химиотерапия перед операцией, также проводится лимфодиссекция, так как риск рецидива в данном случае высокий12.
- Наличие трех и более метастазов в лимфатических узлах по результатам биопсии сторожевых лимфатических узлов, вне зависимости от того, проводилась химиотерапия или нет.
Проводится ли операция при четвертой стадии рака молочной железы?
В некоторых случаях рак молочной железы сразу проявляет себя как метастатическое заболевание. В этой ситуации удаление молочной железы, как правило, не проводится, так как доказательства убедительного влияния на результаты терапии при удалении молочной железы отсутствуют9,12.
Однако, опухоль молочной железы, особенно при неэффективности лекарственной терапии, иногда создает ряд проблем. Достигая больших размеров, опухоль может подвергаться распаду, который сопровождается кровотечением и инфицированием. В этой ситуации рассматривается возможность санитарной или паллиативной мастэктомии, при которой удаление опухоли имеет симптоматический характер и позволяет предотвратить либо справиться с возникшими осложнениями, которые вызваны распадом опухоли.
Резюме
Больше – не всегда лучше: обширный объем операции при раке молочной железы не гарантирует снижение риска смерти от заболевания, поэтому выбор объема операции в настоящее время определяется индивидуально.
Часть пациенток может подвергаться органосохраняющему лечению при условии послеоперационной лучевой терапии. Органосохраняющая резекция возможна, если размеры опухоли позволяют добиться ее радикального удаления и удовлетворительных косметических результатов.
Далеко не всегда пациентки нуждаются в удалении всех подмышечных лимфоузлов. Отсутствие признаков пораженных лимфоузлов перед операцией обосновывает возможность проведении биопсии сигнального лимфоузла и удаления лишь тех узлов, которые копят введенный пациентки радиофармпрепарат. Но, к сожалению, не везде эта процедура возможна и не всегда она предотвращает удаление всех лимфоузлов подмышечной области.
